https://www.163.com/dy/article/FS03NVNC0511BNSN.html
近年来,作为一种主动的肿瘤免疫治疗策略,肿瘤治疗性疫苗引起的抗肿瘤细胞免疫反应在大多数情况下并不理想。产生肿瘤特异性的CD8 T细胞是疫苗发挥作用的关键所在,这个过程涉及对抗原输送到抗原呈递细胞(APC)的时空控制、抗原在抗原呈递细胞中的胞质输送及其交叉呈递。随着越来越多肿瘤新抗原被鉴定以及用于抗原递送的纳米载体被开发,肿瘤纳米疫苗虽然取得了显著的发展,然而开发更有效的肿瘤治疗性疫苗载体是肿瘤疫苗治疗领域的当务之急。

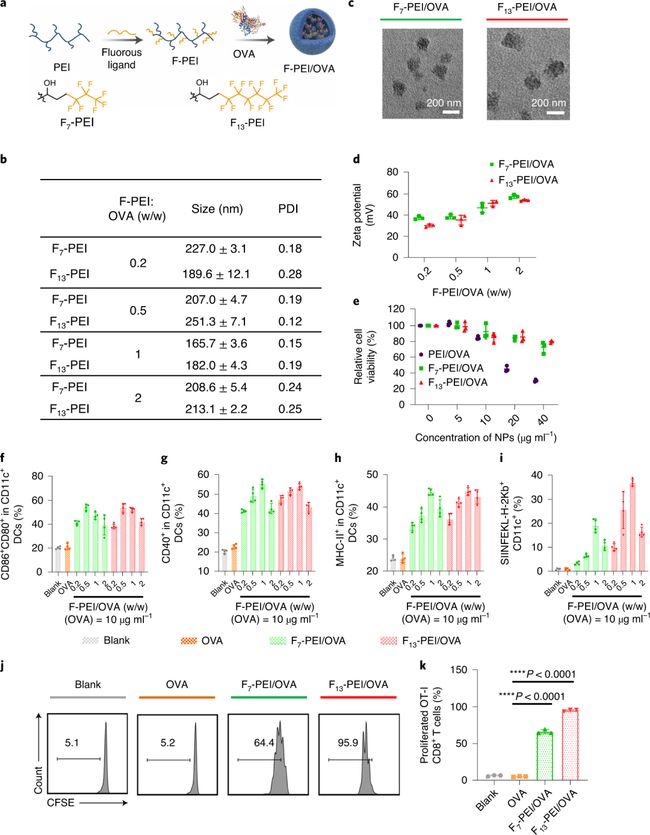
近日,苏州大学功能纳米与软物质研究院刘庄教授、彭睿教授和华东师范大学程义云教授等人在Nature Nanotechnology上在线发表了题目为“A general strategy towards personalized nanovaccines based on fluoropolymers for post-surgical cancer immunotherapy”的研究成果,报道了一种基于氟化高分子(F13-PEI)个性化肿瘤疫苗的构建策略,用于术后肿瘤免疫治疗。经研究发现,F13-PEI与抗原组成的简单复合物不仅可以有效促进抗原在抗原递呈细胞中的胞质输送、显著增强对抗原的交叉呈递,还可以通过激活Toll 样受体4(TLR4)刺激产生细胞因子,从而显著增强该纳米疫苗的抗癌效应。
利用F-PEI包裹肿瘤细胞膜的能力,将F13-PEI与切除肿瘤的癌细胞膜简单混合,即可制备出个性化的抗肿瘤疫苗。在B16黑色素瘤和CT26结肠癌皮下肿瘤模型和自发转移的原位4T1乳腺癌肿瘤模型中证明,F13-PEI/Mem个性化纳米疫苗联合免疫检查点抑制疗法可以治疗术后的远端肿瘤和原位转移肿瘤。此外,在原位4T1肿瘤模型中,他们观察到该联合策略具有强大的免疫记忆效应,可以有效地保护治愈的小鼠免受肿瘤的再次攻击。总体而言,这种基于F-PEI的个体化抗癌疫苗与免疫检查点疗法的协同作用在肿瘤术后的个性化免疫治疗中可能有较大的临床转化价值。
本文第一作者为苏州大学功能纳米与软物质研究院徐骏博士。
本工作得到国家重点研发计划(2016YFA0201200, 2017YFE0131700,2019YFA0904500),国家自然科学基金(51525203, 21725402,51761145041),江苏省社会发展项目(BE2019658),江苏省高等学校自然科学基金(19KJA310008)的资助。
https://www.nature.com/articles/s41565-020-00781-4